Škoda. Stačilo by glazury vnímat podobně, jako ostatní části keramiky. Vždyť nikdo přece nepochybuje, že ovládnutí hrnčířského kruhu vyžaduje určité úsilí. Zrovna tak zvládnutí modelovaného portrétu či nacvičení majolikové malby zabere nějaký čas. Proč by se měly glazury lišit?
Chování glazur můžeme formulovat do řady principů. Pojďme si některé z nich vysvětlit. A vezměme to pěkně od píky.
Definice
Glazuru bychom mohli definovat jako vrstvu nedokonalého skla na povrchu keramiky.
Nedokonalého proto, že sklo je sice amorfní, tedy nekrystalická látka, ovšem v glazurách se zcela běžně ve vyskytuje i celá řada různých krystalů. S výrazem „na povrchu“ to také není úplně jednoznačné, protože mezi střepem a glazurou vzniká různě silná přechodová vrstva, ve které se oba materiály mísí.

Mluvíme-li o skle jako o amorfní látce, máme na mysli jeho zvláštní stav, který se označuje jako tzv. přechlazená tavenina. Vzhledem k tomu, že sklo nedostane dostatek času ke krystalizaci (tedy k pravidelnému uspořádání částic) hovoříme o tavenině i při normálních teplotách. Přestože má přechlazená tavenina značnou viskozitu (vnitřní tření), stále si uchovává omezenou schopnost téct. Pro lepší představu si můžeme uvést příklad cukru, který zahříváním ztrácí svou krystalickou strukturu a mění se na amorfní karamel. Ten během opětovného chladnutí znovu nezkrystalizuje, ale jen ztuhne.
Transparentní glazura
Pokud bychom byli hypoteticky schopni ze skloviny odstranit barvící oxidy a kaliva, pak z jakékoliv lesklé glazury získáme transparentní. Transparentní glazuru pro účely dalšího míchání nazýváme „základ“. Ten může mít mnoho různých vlastností. Liší se především v chemickém složení, což má za následek rozdíly v teplotě tání, koeficientu teplotní roztažnosti, chemické odolnosti, mechanické pevnosti, reakci na barvící oxidy, pecní atmosféru atd.
Kromě výroby a domíchávání transparentních glazur můžeme získat glazuru i jinými metodami, např. tavením nízkotavných jílů (tzv. šlemovky) – článek Barevný svět šlemovek, popelů – více v článku Popely, hornin, aplikací sodných sloučenin do pece při výpalu (solná a sodná glazura) – článek Glazování výpary, nebo krystalizací taviv na povrchu křemičitého střepu (egyptská pasta).
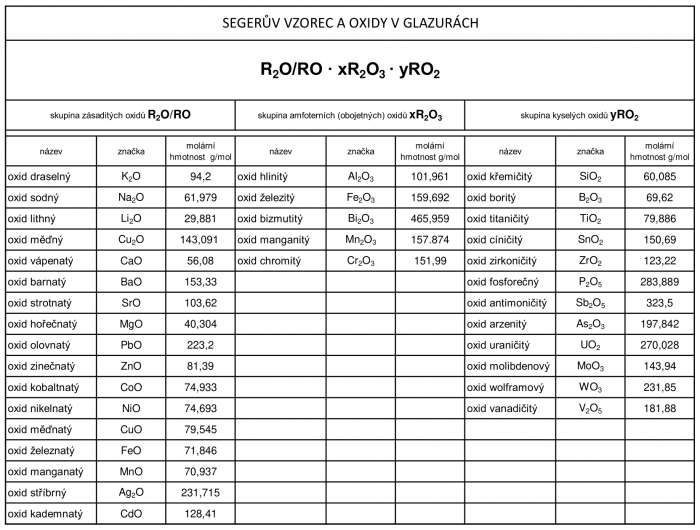
Segerův vzorec
Výpalem se glazura do značné míry přeměňuje. Kromě mnoha jiných změn se z různých sloučenin (solí, uhličitanů, hydroxidů…) stávají oxidy. Německý chemik Hermann August Seger oxidy v glazurách systematizoval a položil tak základy pro dnešní glazurové výpočty. Tzv. Segerův neboli molární vzorec dělí oxidy do tří skupin a určuje mezi nimi jejich molární poměry.
Molárnímu vzorci bývá vytýkána nepřesnost, nicméně se nejčastěji jedná o nepřesnosti v analýzách vstupních surovin. Je třeba si uvědomit, že chemie glazur není o přesné matematice, spíše slouží jako nástroj, který pomáhá při srovnávání jedné věci s druhou a zasazování pozorovaných jevů do souvislostí. Vzorec dále tvoří systém, díky kterému je možné přepočítat a nahradit scházející suroviny v receptuře za takové, které máme. Také lze početně zjistit přibližnou teplotu tání glazury, aniž bychom ji předem vypálili.
Tři skupiny oxidů
Výše zmiňované skupiny v Segerově vzorci jsou kyselé oxidy, taviva a stabilizátory a jsou společné pro drtivou většinu glazur. Nyní si každou zvlášť představíme.
Kyselé oxidy jsou ve vzorci označeny jako yRO2. Jejich zdaleka nejdůležitějším zástupcem je SiO2 – oxid křemičitý. Sám o sobě je schopen tvořit sklo. Potíž je s jeho vysokou teplotou tání, která se pohybuje okolo 1710 °C.
Zásadité oxidy neboli taviva snižují teplotu tání oxidu křemičitého na únosnou mez. Ve vzorci je označujeme jako R2O/RO. V součtu mají vždy číslo 1 a ostatní dvě skupiny se k tavivům vztahují. Mezi nejdůležitější řadíme oxidy vápníku, sodíku, draslíku, hořčíku, olova a lithia. Druh taviva a jeho množství určuje ve sklovině spoustu důležitých vlastností, mezi které patří teplota tání, sklon k harisování (trhlinkování), chemická odolnost, mechanická pevnost, pružnost, viskozita, sklony k odskelnění (krystalizaci) apod. Do skupiny taviv také patří celá řada barvících oxidů.
Amfoterní (obojetné) oxidy neboli stabilizátory se nacházejí uprostřed Segerova vzorce s označením xR2O3. Na prvním místě stojí Al2O3. Přestože se u nízkotavných olovnatých glazur někdy nepoužívá, tak ve většině případů je nedílnou složkou stabilizující sklovinu a bránící krystalizaci. Ve formě jílů zamezuje sedimentaci glazurové suspenze.
Proto, aby byla glazura glazurou, je nezbytné vyvážené zastoupení oxidů z každé skupiny, a právě k tomu slouží Segerův vzorec.

Vzorkovnice na obrázku je příkladem toho, jak funguje rovnováha mezi kyselou, amfoterní a zásaditou složkou glazury. Množství a druh zásaditých oxidů se v jednotlivých testech nemění. Jak už bylo zmíněno výše, jejich součet se z početních důvodů vždy rovná jedné. Směrem doprava přibývá kyselé složky tedy SiO2. Odspoda nahoru přibývá stabilizační složky tedy Al2O3. A aby to nebyla jen nudná transparentní glazura, tak každý vzorek obsahuje 8 % oxidů železa. Páleno 1350 °C v redukci na technickém porcelánu.
Každá ze skupin se při předávkování projevuje jinak. Velká množství SiO2 vpravo dole již netvoří dostatek skloviny. Velká množství Al2O3 vlevo nahoře vytvářejí v podstatě povrchy podobné engobám. Vlevo dole mají jehlánky na vzorkovnici v poměru k ostatním největší obsah zásaditých oxidů, což vede ke stékání a intenzivní krystalizaci některých taviv.
Suroviny
Již na první pohled je patrné, že tato surovina obsahuje hned tři oxidy ze skupiny taviv, jeden ze skupiny stabilizátorů a jednu složku sklotvornou. Přidáme-li tedy takový živec do glazury, vnášíme do ní 5 oxidů ze všech tří skupin. Pokud by receptura naší hypotetické glazury neobsahovala jeden jediný oxid obsažený v živci, pak jej nemůžeme použít a musíme se poohlédnout po jiné surovině. A to je důvod, proč je tak důležité, dobře znát glazurové suroviny.
Eutektikum
Tento v souvislosti s glazurami používaný pojem byl už vysvětlen v článku zabývajícím se tavivy ve hmotách. Ostatně hmoty a glazury toho mají společného více, než je na první pohled patrné. Více se dočtete zde:
Žárovzdorné materiály v ateliérové keramice I
Nad rámec odkazovaného textu pro porovnání připojuji tabulku eutektických bodů (nejnižších možných teplot tání) dalších třísložkových soustav. Například glazury v soustavě K2O·Al2O3·SiO2 začínají fungovat již od 695 °C.
| soustava | teplota tání |
| K2O·Al2O3·SiO2 | 695 °C |
| Na2O·Al2O3·SiO2 | 732 °C |
| Li2O·Al2O3·SiO2 | 975 °C |
| CaO·Al2O3·SiO2 | 1170 °C |
| BaO·Al2O3·SiO2 | 1250 °C |
| MgO·Al2O3·SiO2 | 1355 °C |
| SrO·Al2O3·SiO2 | 1400 °C |
Závěr
V podstatě nejobtížnějším problémem glazur je nekonečné množství kombinací mezi surovinami, vrstvami, pálícími teplotami, křivkami, pecní atmosférou, podkladovým materiálem apod. Proto je výhodné používat systémy, které vznikající kombinace třídí. Na Západě se o to celkem úspěšně pokusil pan Seger. Je možné i prosté kombinování každého s každým, ostatně na Východě keramici postupovali právě tak – čistě empiricky. Nicméně dosažení současné úrovně poznání trvalo východoasijským hrnčířům 3500 let.
Ať zvolíme jakoukoliv z cest, začátek může být obtížný a leckdy se ztratíme. Štěstí popřeje každému, komu občasné zabloudění nevadí a nalézá radost i v cestě samé. Kéž se prvotní prodírání trnitým hložím brzy změní na radostný výlet malebnou krajinou.
Citace:Bloomfield, Linda. Science for Potters. The American Ceramic Society, 2018.https://digitalfire.com/material/253, 26.6.2020
Autor: Petr Toms | Jazyková korektura: Zuzana Chomátová


Přihlaš se a vlož komentář...